Cell:阿尔茨海默病侵蚀了脑细胞对基因表达的控制,破坏了功能和认知
时间:2025-09-24
来源:100医药网 2025-09-24 15:11
阿尔茨海默病不仅仅是关于斑块和缠结,而是关于细胞核秩序本身的侵蚀。大多数人通过其破坏性症状(如记忆丧失)来认识,而新药则针对疾病表现的病理方面,例如淀粉样蛋白斑块。如今,麻省理工学院研究人员在《细胞》杂志上发表的一项全面的新研究,揭示了将该疾病理解为一场关于脑细胞如何控制其基因表达的斗争的重要性。

这项研究描绘了一幅高分辨率的图景,展现了为维持健康的基因表达和基因调控而进行的 殊死搏斗,在这场搏斗中,失败或成功的后果无异于细胞功能和认知能力的丧失或保存。
该研究首次呈现了一个多模态图谱,它结合了基因表达和基因调控信息,涵盖了来自六个大脑区域的350万个细胞,这些数据是通过分析111位捐赠者的384份死后大脑样本获得的。研究人员不仅分析了"转录组"(显示哪些基因被表达成了RNA),还分析了"表观基因组"(一套染色体修饰,决定了哪些DNA区域是可接近的,从而在不同细胞类型中被利用)。
由此产生的图谱揭示了许多见解,表明阿尔茨海默病的进展以两大表观基因组趋势为特征。第一,关键大脑区域中的易损细胞,其细胞核内严格的"区室"结构遭到破坏。细胞通常维持这些区室以确保基因组的某些部分开放表达,而其他部分则被锁定。
第二个主要发现是,易感细胞经历了"表观基因组信息"的丢失,这意味着它们失去了对基因调控和表达独特模式的掌控,而这种模式赋予了它们特定的身份并保障了其健康功能。
除了区室化受损和表观基因组信息侵蚀的证据外,还有许多具体发现精确指出了按细胞类型、大脑区域和基因网络分类的分子回路是如何崩溃的。例如,他们发现,当表观基因组条件恶化时,就为许多与疾病相关的基因的表达打开了大门;而如果细胞能够设法维持其表观基因组的秩序,就能抑制疾病相关基因。此外,研究人员清楚地看到,当表观基因组崩溃发生时,人们会丧失认知能力,但在表观基因组稳定性得以维持的地方,认知能力也得以保存。
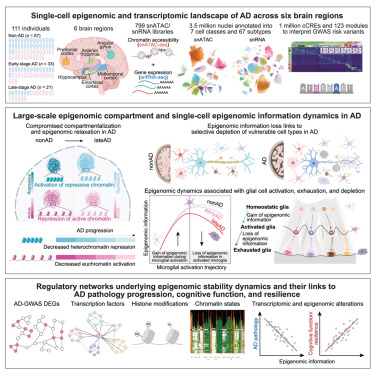
"要理解导致阿尔茨海默病(AD)基因表达变化的回路和逻辑,我们需要理解所有正在发生的变化的调控和上游控制,这就是表观基因组发挥作用的地方,"该研究的资深作者、计算机科学与人工智能实验室教授、麻省理工学院计算生物学组负责人Manolis Kellis说。"这是首个大规模、单细胞、多区域的AD基因调控图谱,系统剖析了跨疾病进展和韧性时期的表观基因组和转录组程序的动态变化。"Kellis实验室成员Zunpeng Liu和Shanshan Zhang是该研究的共同第一作者。
通过对阿尔茨海默病进展的表观基因组机制进行如此详细的检查,该研究为设计新的阿尔茨海默病疗法提供了蓝图,这些疗法可以针对导致表观基因组控制广泛侵蚀的因素,或针对影响关键细胞类型(如神经元和支持性胶质细胞)的具体表现。
"开发新的、更有效的阿尔茨海默病治疗方法的关键,取决于我们加深对导致大脑细胞和网络功能崩溃机制的理解,"共同通讯作者Li-Huei Tsai说,"这些新数据增进了我们对表观基因组因素如何驱动疾病的理解。"
受损的区室与侵蚀的信息
该研究中的死后大脑样本,有57份来自"宗教 Orders 研究"或"拉什记忆与项目"(合称"ROSMAP")的捐赠者,这些捐赠者没有AD病理或症状;33份来自具有早期病理的捐赠者;21份来自处于晚期的捐赠者。因此,这些样本提供了关于每位捐赠者在生前所经历的症状和病理的丰富信息。
在这项新研究中,Liu和Zhang结合了对样本的单细胞RNA测序分析和ATACseq分析。前者测量每个细胞中哪些基因正在被表达,后者测量染色体区域是否可供基因表达。
将这两种转录组和表观基因组测量方法结合起来,使研究人员能够理解分子细节,了解七大类脑细胞(如神经元或其他胶质细胞类型)和67种细胞亚型(如17种兴奋性神经元或6种抑制性神经元)中基因表达是如何被调控的。
研究人员注释了超过100万个基因调控控制区,不同的细胞利用表观基因组标记来建立其特定的身份和功能。然后,通过将阿尔茨海默病患者大脑中的细胞与健康大脑中的细胞进行比较,并考虑病理阶段和认知症状,他们能够严格地关联这些表观基因组标记的侵蚀与最终的功能丧失。例如,他们发现,在进展到晚期AD的人群中,通常是抑制性的区室开放以便进行更多表达,而在健康时期通常更开放的区室则变得更加抑制。令人担忧的是,当脑细胞通常的抑制区室开放时,它们更容易受到疾病的影响。
"对于阿尔茨海默病患者,抑制区室开放了,基因表达水平增加,这与认知功能下降相关,"第一作者Zunpeng Liu解释道。但是,当细胞设法保持其区室有序,使其表达本该表达的基因时,人们就能保持认知完整。
同时,根据细胞对其调控元件的表达,研究人员为每个细胞创建了一个表观基因组信息评分。总的来说,随着病理的进展,信息会减少,但在阿尔茨海默病中最先受影响的两个大脑区域(内嗅皮层和海马体)的细胞中,这一点尤其显著。分析还强调了特别易感的特定细胞类型,包括发挥和其他作用的小胶质细胞、为神经元产生髓鞘绝缘体的少突胶质细胞,以及特定类型的兴奋性神经元。
风险基因与"染色质守护者"
这篇论文中的详细分析强调了表观基因组调控如何与疾病相关问题相关联,Liu指出。例如,APOE基因的e4变体被广泛认为是阿尔茨海默病最大的单一遗传风险因素。在APOE4大脑中,小胶质细胞最初对出现的疾病病理反应是表观基因组信息的增加,这表明它们正在挺身而出履行其抗击疾病的独特责任。但随着疾病的进展,这些细胞的信息量急剧下降,这是恶化和变性的迹象。这种转变在拥有两个APOE4拷贝(而非一个)的人身上最为强烈。Kellis说,这些发现表明APOE4可能使小胶质细胞的基因组不稳定,导致其衰竭。
另一个例子是表达RELN基因及其蛋白Reelin的神经元的命运。先前的研究(包括Kellis和Tsai的研究)表明,内嗅皮层和海马体中表达RELN的神经元在阿尔茨海默病中特别脆弱,但如果它们存活下来则能促进韧性。这项新研究通过证明这些神经元随着疾病进展表现出早期且严重的表观基因组信息丢失,但在保持认知韧性的人中,这些神经元维持了表观基因组信息,从而为它们的命运提供了新的线索。
在另一个例子中,研究人员追踪了他们通俗称为"染色质守护者"的因子,因为它们的表达维持和调控细胞的表观基因组程序。例如,表观基因组侵蚀更严重和AD进展更快的细胞,在本应由Polycomb抑制基因或其他基因表达沉默子锁定的区域,表现出染色质可及性增加。而有韧性的细胞表达促进神经连接性的基因,表观基因组被侵蚀的细胞则表达与炎症和氧化应激相关的基因。
"信息很明确:阿尔茨海默病不仅仅是关于斑块和缠结,而是关于细胞核秩序本身的侵蚀,"Kellis说。"当染色质守护者在侵蚀的力量面前失守,在基因组调控的最基本层面从韧性转向脆弱时,认知衰退就出现了。当我们的脑细胞在其最深处 我们的神经元和小胶质细胞内部 失去它们的表观基因组记忆标记和表观基因组信息时,阿尔茨海默病患者似乎也在最高层面失去了他们的记忆和认知能力。"(100yiyao.com)
参考文献:
Zunpeng Liu et al, , Cell (2025). DOI: 10.1016/j.cell.2025.06.031.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载->
