2025 ASCO:CheckMate 816/77T携两大LBA,试图解答能不能做“精准辅助治疗” !
时间:2025-06-07
来源:奇点糕 2025-06-07 15:08
CheckMate-816中近1/4的pCR率和该人群95%的5年OS率无疑为这一领域树立了全新的疗效标准,这一里程碑数据将推动学术界聚焦更多细分人群的治疗策略。可手术非小细胞()的治疗,可以说是近几年癌症领域内的 兵家必争之地 。基于以CheckMate-816/CheckMate-77T为代表的多项关键临床研究结果,新辅助(术前)、辅助(术后)、围术期(术前+术后)三种不同免疫治疗方案正呈 三足鼎立之势 ,都在临床实践中被广泛应用。但另一方面,这一领域其实还存在许多不确定性。比如,每种治疗方案的适用患者、可指导用药和预测疗效的标志物,乃至长期临床获益的确切证据都还没有被充分确立,而由于缺少头对头临床研究,哪种免疫治疗方案应居于优选地位,当前更是悬而未决。
然而,从刚刚落幕的2025美国临床肿瘤学会()年会上,公布的两项关键临床III期研究最新分析结果[1-2]中,我们或许可以找到部分问题的答案:一方面,全球首个免疫新辅助治疗III期研究CheckMate-816率先公布了其5年随访数据,惊艳地证实仅三周期新辅助免疫治疗+化疗,即可带来具有学意义的总生存期(OS)改善,进一步夯实了这一模式的核心地位;不仅如此,采用围术期模式的CheckMate-77T研究也公布了生存数据更新和生物标志物分析,两者共同为围术期免疫治疗的应用提供了重要依据。
双双位列LBA级成果,长生存数据+标志物分析将成为关键指引相继登上《新英格兰医学杂志》[3-4],足以说明CheckMate-816/77T两项研究的分量有多重,而作为围术期免疫治疗走得最快的一批临床研究,本次亮相ASCO年会的是CheckMate-816研究最终OS分析结果和CheckMate-77T研究的最新生存数据,以及循环肿瘤DNA(ctDNA)清除、病理学完全缓解(pCR)方面的探索性分析结果,两项结果均作为LBA级摘要,在大会上以口头报告形式公布(摘要号:LBA8000、LBA8010)。
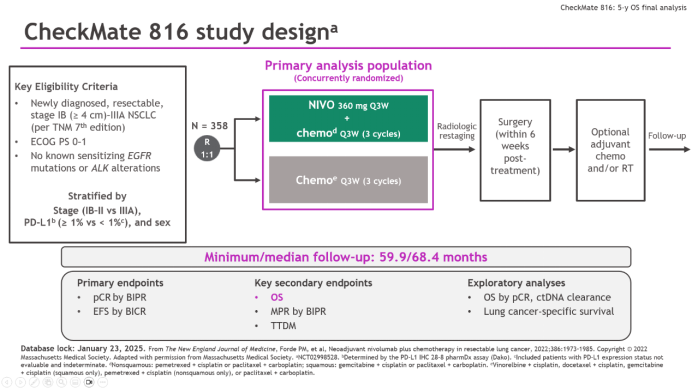
CheckMate-816回顾
先说CheckMate-816研究的情况,本次更新最终OS分析结果时,患者中位随访时间达68个月(范围: 60 85个月),纳武利尤单抗+化疗方案作为术前新辅助治疗,继续保持了相较单纯化疗的OS获益,风险比(HR)值为0.72(95% CI: 0.523-0.998, P=0.0479),达到了预设的统计学显著性界值;两组患者5年OS率分别为65%和55%,且各预设亚组中OS数据均呈现出获益趋势。
上述数据使CheckMate-816研究成为首个报告5年长生存获益的免疫新辅助治疗临床III期研究,也是目前所有免疫治疗用于实体瘤的III期研究中,唯一仅通过免疫新辅助治疗取得OS显著改善的研究,结果也同步发表在了《新英格兰医学杂志》上[5]。
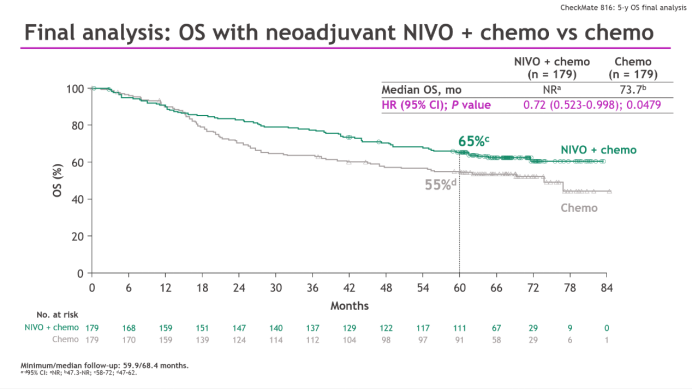
CheckMate-816研究最终OS分析结果
无事件生存期(EFS)方面,纳武利尤单抗+化疗组的长期获益同样稳健(HR=0.68),5年EFS率为49%,较化疗组(34%)改善15%,近一半患者实现了5年无复发进展生存,即接近临床上常用的 治愈 目标。
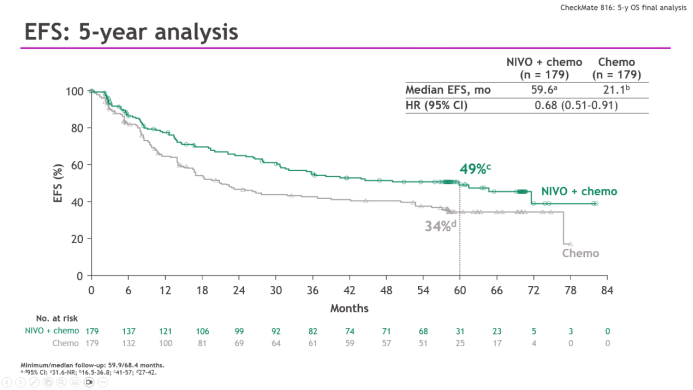
CheckMate-816研究5年EFS分析结果
pCR探索性分析的结果同样引人注目:在纳武利尤单抗+化疗组中,达到pCR患者的5年OS率高达95%,死亡风险较未达到pCR的患者降幅高达近90%(HR=0.11,non-pCR患者5年OS率为56%);在EFS方面也观察到了相似的结果,pCR患者5年EFS率达88%(non-pCR患者:35%,HR=0.14)。
同时,CheckMate-816研究也设置有ctDNA和pCR与疗效关系的探索性分析,对86例基线时ctDNA阳性(两组各43例)患者的分析显示,完成新辅助治疗后纳武利尤单抗+化疗组和化疗组的ctDNA清除率分别为56%和35%,而两组中实现ctDNA清除的患者,相比未清除患者均有明显OS获益(纳武利尤单抗+化疗组HR=0.38,化疗组HR=0.39)。
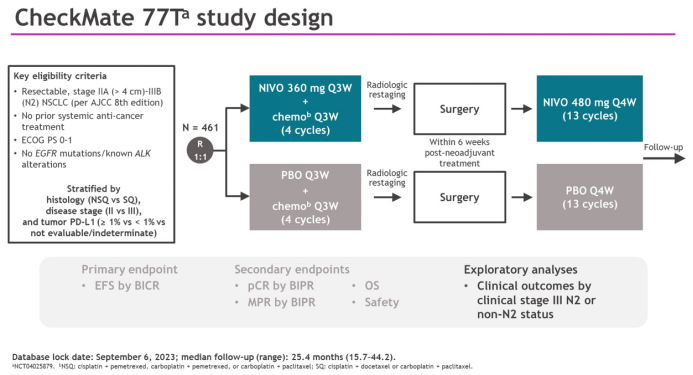
CheckMate-77T研究设计回顾
而CheckMate-77T研究的最新数据也不遑多让:本次更新数据为中位随访41.0个月时的结果,纳武利尤单抗组较安慰剂组继续保持了优秀的EFS获益(HR=0.61, 95% CI: 0.46-0.80),两组30个月EFS率分别为61%和43%,且所有随机分组患者,不同疾病分期、肿瘤组织学类型或PD-L1表达水平亚组均呈一致趋势;同时在首次预设的OS分析中,纳武利尤单抗组已初步显现OS改善的趋势(HR=0.85, 30个月OS率: 78% vs. 72%)。
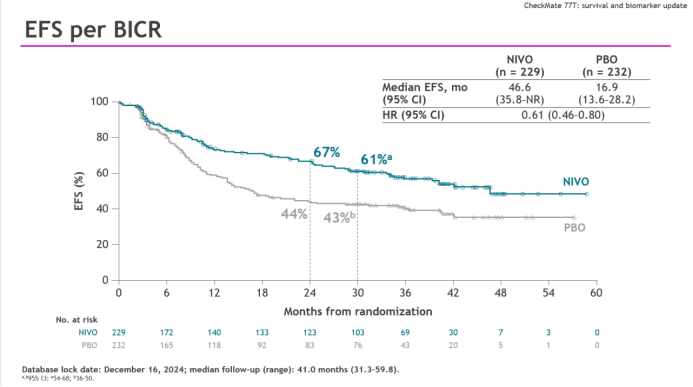
CheckMate-77T研究EFS数据更新结果
探索性分析中,纳武利尤单抗组相比安慰剂组在达到pCR患者中的EFS HR=0.90(自根治性手术后的Landmark EFS),在non-pCR患者中EFS HR=0.72;在190例可评估生物标志物的患者(纳武利尤单抗组98例,安慰剂组92例)中,无论是否达到pCR,基线及术前ctDNA清除患者都有更明显的EFS获益(纳武利尤单抗组HR=0.41,安慰剂组HR=0.62);纳武利尤单抗的获益也不受是否合并KRAS、STK11和/或KEAP1突变影响。
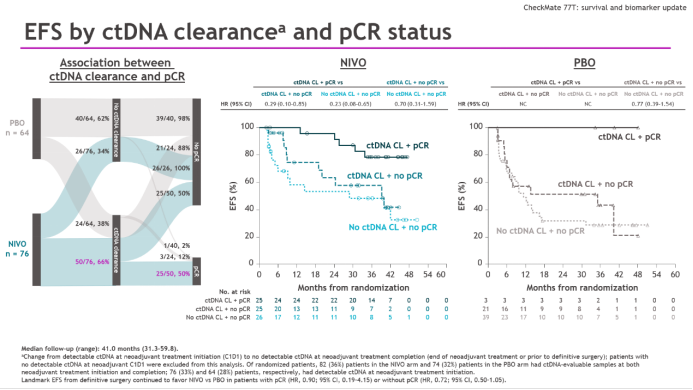
CheckMate-77T研究基于pCR状态/ctDNA清除情况划分的患者EFS数据
减少 摸着石头过河 式尝试,围术期精准免疫治疗或已不再遥远虽然在过去几年中,可手术NSCLC的围术期免疫治疗临床III期研究结果堪称 井喷式 公布,但许多备受学界关注的问题仍然没有答案,比如:国内外权威推荐的免疫新辅助、辅助、围术期治疗适用人群范围存在明显重合(即都包括肿瘤直径 4cm或淋巴结阳性患者),然而尚不能对哪类患者适用何种方案继续细化推荐;一些现有的推测、观点和跨研究分析也都有着很强的 摸着石头过河 意味。
在这样的背景下,本次ASCO年会公布的CheckMate-816和CheckMate-77T分析结果的意义,就在于其首次在III期研究的长期(3~5年)随访数据中,通过pCR、ctDNA等关键指标,为新辅助治疗后患者的精准分层提供了实质性的依据。
首先,pCR这一指标的预后价值得到了强有力的验证。CheckMate-816的5年随访数据证实,新辅助免疫联合化疗后达到pCR的患者5年OS率高达95%,EFS率达88%,死亡风险和EFS风险较non-pCR患者均降低近90%(OS HR=0.11,EFS HR=0.14),表明pCR患者已相当接近一般意义上的 临床治愈 ,或可免于后续辅助治疗,避免过度治疗。这一结果进一步凸显了pCR在该类患者临床决策中的核心地位,未来临床研究或也可将pCR作为关键替代终点,加速药物研发。
其次,两项研究均系统评估并强烈提示了ctDNA与长期预后的相关性。ctDNA是释放至血液中的游离DNA片段,可用于监测微小残留病灶(MRD),预示复发风险;其检测技术于2010年后快速发展,优点在于、便捷,可实时反映治疗应答和疾病进展。
CheckMate-816研究中,新辅助免疫+化疗后ctDNA清除率不仅对比化疗更高,且清除患者的OS对比未清除患者明显改善;CheckMate-77T研究数据则进一步显示,无论是否达到pCR,围术期ctDNA清除患者的EFS获益均更大。这些数据表明,ctDNA动态监测是传统病理评估的重要补充,期待未来随着技术灵敏度和临床可及性的提升,ctDNA能成为围术期精准治疗的关键调控指标。
而在non-pCR人群的治疗决策方面,两项研究结果也给出了重要参考依据。首先,CheckMate-77T的分析结果显示,围术期模式对此类患者表现出额外获益(非pCR患者自根治性手术的landmark EFS HR=0.72);且2024年世界肺癌大会(WCLC)上公布的一项CheckMate-816和CheckMate-77T研究间的患者个体层面的倾向性评分加权分析也显示(围术期免疫治疗对比新辅助免疫+化疗的EFS HR=0.61)[6],non-pCR患者可能较需要免疫辅助治疗(尤其是PD-L1阴性患者,其EFS HR=0.51)。
此外,如前所述,ctDNA对于non-pCR患者的进一步分层也具有指导价值,如可将non-pCR患者进一步细分为ctDNA阳性和阴性,指导辅助治疗决策(CheckMate-77T接受纳武利尤单抗+化疗后non-pCR患者中,ctDNA清除对比非清除患者的EFS HR=0.70)。也有观点指出,原发耐药患者(如新辅助免疫+化疗后仍有较多肿瘤残留、ctDNA持续阳性)从免疫辅助治疗中的获益可能有限[7],未来还需探索进一步的替代策略。
整体来看,结合现有证据,当下针对可手术NSCLC患者的治疗方案的选取或将介于CheckMate-816和CheckMate-77T模式之间,并不严格归一。例如,患者在接受纳武利尤单抗+化疗新辅助治疗并完成手术后,可根据其分期、病理残留和ctDNA等因素综合考虑后续是否行辅助治疗及时长,以最小代价实现最大获益。也十分期待这一领域能有前瞻性随机对照研究的开展以进一步验证这一路径,并进一步优化生物标志物指导下的个体化治疗。
总之,CheckMate-816中近1/4的pCR率和该人群95%的5年OS率无疑为这一领域树立了全新的疗效标准,相信这一里程碑数据将推动学术界聚焦更多细分人群的治疗策略,最终使更多患者朝着 5年生存率95% 这一理想目标迈进。
参考文献:
[1]Forde P M, et al. Overall survival with neoadjuvant nivolumab + chemotherapy in patients with resectable NSCLC in CheckMate 816. Presented at: American Society of Clinical Oncology Annual Meeting (ASCO 2025); May 30-June 3, 2025; Chicago, IL, USA. Abstract LBA8000.
[2]Cascone T, et al. Perioperative nivolumab vs placebo in patients with resectable NSCLC: updated survival and biomarker analyses from CheckMate 77T. Presented at: American Society of Clinical Oncology Annual Meeting (ASCO 2025); May 30-June 3, 2025; Chicago, IL, USA. Abstract LBA8010.
[3]Forde P M, Spicer J, Lu S, et al. Neoadjuvant nivolumab plus chemotherapy in resectable lung cancer[J]. New England Journal of Medicine, 2022, 386(21): 1973-1985.
[4]Cascone T, Awad M M, Spicer J D, et al. Perioperative nivolumab in resectable lung cancer[J]. New England Journal of Medicine, 2024, 390(19): 1756-1769.
[5]Forde P M, et al. Overall Survival with Neoadjuvant Nivolumab plus Chemotherapy in Lung Cancer. New England Journal of Medicine, Published June 2, 2025.
[6]Forde P M, Peters S, Donington J, et al. PL02. 08 perioperative vs neoadjuvant nivolumab for resectable NSCLC: patient-level data analysis of CheckMate 77T vs CheckMate 816[J]. Journal of Thoracic Oncology, 2024, 19(10): S2.
[7]Phillips W J, Jackson A, Kidane B, et al. Immunotherapy for early-stage non-small cell lung cancer: A practical guide of current controversies[J]. Clinical Lung Cancer, 2025, 26(3): 179-190.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载->
