PD-(L)1角逐新战场
时间:2025-09-22
来源:医药魔方 2025-09-22 14:00
从PD-1的最初发现到如今的临床广泛应用,这一靶点的发展历程充分诠释了基础科学发现的巨大价值。更令人兴奋的是,PD-(L)1靶点的创新潜力远未触及天花板。近日,外媒传出复宏汉霖正在与强生、罗氏等跨国药企洽谈PD-L1 ADC的权益许可事宜,首付款可能高达数亿美元,这一消息再次印证了PD-(L)1靶点的巨大研发价值和市场潜力。
作为调节的 刹车系统 ,PD-1/PD-L1通路已成为抗肿瘤药物开发中最富创新价值的领域之一。从最初的PD-(L)1单抗到如今备受关注的PD-(L)1双抗以及正在探索的多抗、ADC药物形式,这一靶点持续为提供全新的药物开发思路。除了抑制PD-1/PD-L1通路,激动PD-1/PD-L1通路的策略也正试图在自身免疫性疾病领域开辟全新的治疗天地。
PD-(L)1所蕴藏的可能性,不断刷新大家的认知。
治疗:PD-(L)1单抗迭代
PD-(L)1单抗彻底改变了肿瘤临床治疗格局,但这仅仅是PD-(L)1药物价值释放的开篇。一方面,在当前临床实践中,耐药性、异质性等挑战依然显著,诸多患者未获得持久有效的获益。这些未被满足的临床需求,从根本上驱动着PD-1/PD-L1策略持续向更、更高效的方向演进。
另一方面,代表性PD-(L)1单抗,如帕博利珠单抗等,其专利将在未来几年内陆续到期,为了平稳度过专利悬崖,押注下一代PD-(L)1疗法已经成为了众多药企不约而同的一种战略选择,毕竟像PD-(L)1这样的超级靶点实属稀缺,许多企业针对该靶点积累了深厚的研发经验,进一步发掘价值也顺理成章。
根据医药魔方数据库,全球PD-(L)1在研创新药已经超过900款,其中双抗类型的药物数量已居第一,是单抗的3倍之多。这一结构性变化表明,业界充分看好PD-(L)1药物从单抗向单抗迭代的策略。
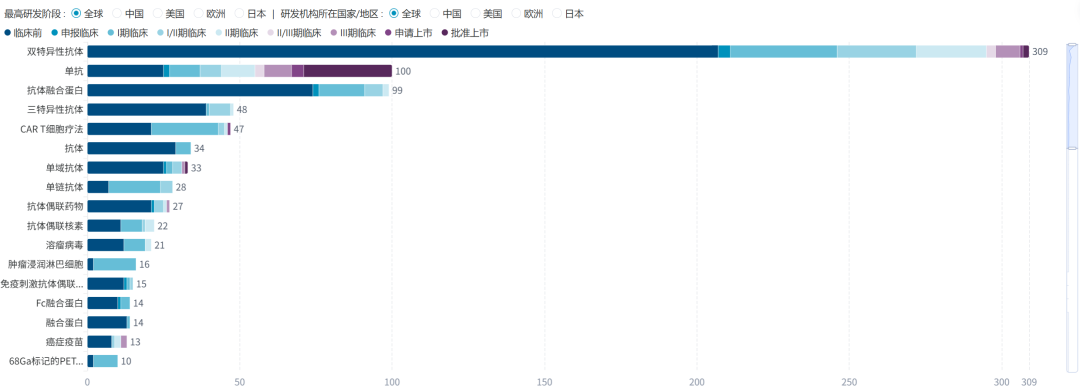
全球PD-(L)1在研创新药的药物类型TOP17
作用机制是这一迭代策略的底层逻辑。同时靶向PD-(L)1和VEGF、4-1BB、CTLA-4等肿瘤相关通路,不仅能够实现协同增效,也能通过阻断肿瘤逃逸的替代通路来降低单一靶点耐药风险。
在众多组合中,PD-(L)1/VEGF双抗成为了当前迭代浪潮中的领先方向。依沃西单抗已经在一项头对头研究中显示优效于帕博利珠单抗[1],初步验证双抗迭代思路的可行性。围绕这一技术路线的BD热潮也随之兴起,包括辉瑞和BMS这样的制药巨头也不惜重金布局,以防错失机遇。
除此之外,其他潜力双抗组合也值得关注,比如PD-L1/TGF- 双抗。恒瑞的瑞拉芙普- 在一线场景取得15.8个月的总生存期(OS)获益[2],有望以此撕开上市突破口;正大天晴的TQB2868则是锁定 癌中之王 发起III期研究[3],期待后续数据读出。
当双抗还在如火如荼迭代研发之际,技术难度更高的PD-(L)1多抗赛道也已悄然启航。比较有代表性的包括基石的PD-1/CTLA-4/VEGF-A三抗CS2009、BioNTech的PD-L1/VEGF/TGF- 三抗PM8003、百利天恒的PD-L1/4-1BB/CD3/CD19四抗Emfizatamab等均已率先进入I/II期临床阶段,该技术路线或将有望突破PD-L1低表达或阴性患者的治疗瓶颈。
从单抗到双抗再到多抗纵深迭代的同时,也有玩家横向拓展开发思路,尝试将强杀伤的ADC药物类型与肿瘤广泛表达的PD-L1靶标进行差异化匹配,以实现更广谱的抗肿瘤作用。
复宏汉霖和辉瑞在这一技术路线上率先取得亮眼成绩,HLX43和PF-08046054[4, 5]已经在早期研究中展现出令人鼓舞的疗效和安全性特征。近期更新的数据显示,HLX43在PD-L1阴性患者人群中的ORR为38.1%[6],提示其抗肿瘤活性或许并不依赖于PD-L1表达水平。在未来的应用路径中,PD-L1 ADC有机会惠及更广泛的患者人群。
自免:PD-(L)1开启新篇
在PD-(L)1抑制剂在肿瘤治疗领域大放异彩的同时,一些具有颠覆性思维的科学家开始探索一个全新的可能:既然阻断PD-(L)1通路可以激活免疫系统对抗肿瘤,那么反向操作 也就是激活这一通路是否能够抑制过度活跃的免疫反应,从而为自免疾病开辟全新的治疗路径?
这种 反向思维 的逻辑基础非常清晰。自免疾病本质上是免疫系统的 刹车失灵 ,导致免疫细胞错误地攻击自身的正常细胞和组织。如果能够重新激活PD-1/PD-L1这个天然的 刹车系统 ,理论上就能够让失控的T细胞回归平衡状态,恢复免疫系统的精准调控能力。
基于这一理念,PD-1/PD-L1通路激动剂开始进入药物科学家的视野,一个全新的治疗领域正在悄然崛起。已经有多家企业在这一前沿赛道布局,来自AnaptysBio、强生等公司的数款激动剂产品已进入不同临床阶段。
临床在研PD-1/PD-L1通路激动剂
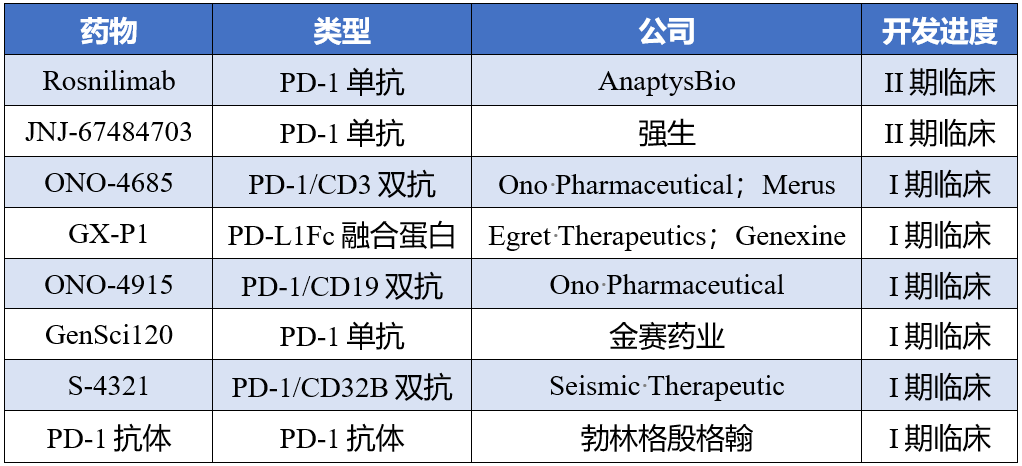
Rosnilimab是目前进展最快的一款PD-1激动剂,已经在II期研究中展现出对(RA)的治疗潜力 其12周治疗数据与已上市药物的24周治疗数据接近[7]。强生的PD-1单抗JNJ-67484703虽然没有在RA人群中取得有学意义的结果,但至少证明了该药物能够有效消耗PD-1阳性T细胞[8]。
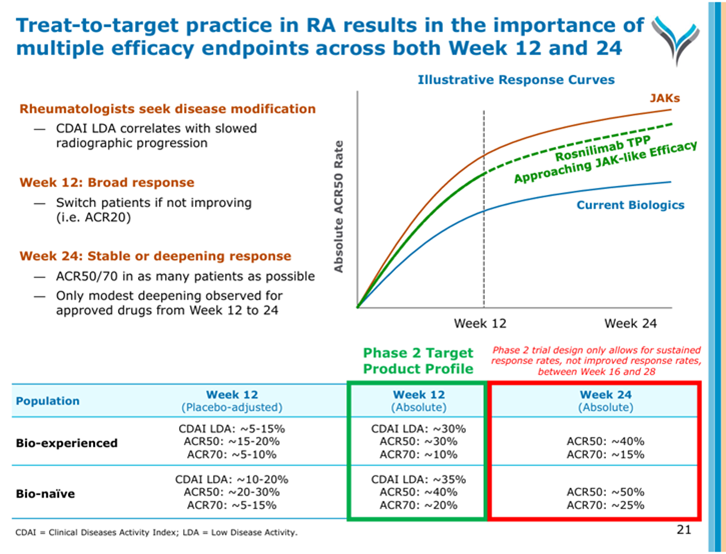
来源:AnaptysBio官网PPT
PD-1/PD-L1通路激动剂相比传统自免药物具有独特的机制优势。目前已上市的自免药物,如IL-17A抑制剂、TNF- 单抗、IL-23p19单抗等,通常是针对炎症反应的下游产物 细胞因子。这些药物虽然能够有效控制炎症症状,但往往难以从根本上调节产生这些细胞因子的免疫细胞本身。
相比之下,靶向激活PD-1/PD-L1通路从而直接调节免疫细胞有望实现更为彻底的治疗效果。更重要的是,这种调控方式相对温和,不会完全抑制免疫功能,可保留正常免疫防御能力。
不过,这一新兴领域的发展也面临着不少挑战。首先,如何找到有效性和安全性的最佳平衡点是一个关键问题,激动不足可能导致疗效不佳,而过度激动则可能引发免疫抑制相关的副作用;其次,不同自免疾病的病理机制存在差异,PD-1/PD-L1通路激动剂对哪些自免疾病更有效还需要更多临床数据支持。此外,激动剂与其他免疫调节药物的联合使用策略也有待深入研究。
总结
从PD-1的最初发现到如今的临床广泛应用,这一靶点的发展历程充分诠释了基础科学发现的巨大价值。更令人兴奋的是,PD-(L)1靶点的创新潜力远未触及天花板。
在肿瘤治疗领域,双抗、多抗、ADC等新技术的不断涌现正在拓展PD-(L)1药物的治疗边界。在自免疾病领域,激动剂策略的探索为这类难治性疾病提供了全新的治疗思路。PD-(L)1靶点应用从肿瘤到自免的跨越也证明了基础科学发现的价值可以通过不断创新而持续放大。
随着双抗、多抗、ADC等新技术平台的不断成熟,PD-(L)1这座 宝矿 还有更多宝藏等待挖掘。未来,我们也将见证更多基于PD-(L)1开发的创新疗法从实验室走向临床,为肿瘤和自身免疫性疾病患者带来新的希望。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载->
