Cancer Cell:科学家识别出癌细胞中特殊的代谢机制 或能提供改善癌症免疫疗法疗效的新靶点
时间:2024-11-27
来源:100医药网 2024-11-27 11:56
本文研究中,研究人员识别出了肿瘤和肿瘤相关巨噬细胞之间通过SLC13A3-衣康酸-NRF2- SLC7A11轴所发生的相互作用,这或许能作为肿瘤微环境中此前未知的免疫铁死亡耐受机制。系统是癌症疗法的主要目标,免疫检查点抑制剂和细胞疗法能显著改善很多癌症患者的治疗结局,但对于大约70%的癌症患者而言,这些疗法或许并没有发挥作用。近日,一篇发表在国际杂志Cancer Cell上题为 Itaconate transporter SLC13A3 impairs tumor immunity via endowing ferroptosis resistance 的研究报告中,来自密歇根大学Rogel癌症中心等机构的科学家们通过研究揭示了为何一些癌症对免疫疗法并不会产生反应,即肿瘤微环境中的代谢转运体会阻断一种对免疫反应非常重要的关键类型的死亡。
研究者Weiping Zou博士说道,肿瘤细胞能调整其代谢机制来躲避基于免疫的疗法,理解这些免疫抵抗机制是如何发挥作用的或能提供新靶点来改进基于免疫的疗法从而让更多患者获益,我们的研究发现就是朝着这一方向迈出的重要一步。文章中,研究人员发现,SLC13A3或能作为肿瘤细胞中代谢产物衣康酸(itaconate)的一种转运体,从而促使细胞对铁死亡(ferroptosis)耐受,铁死亡是一种受调节的细胞死亡形式,此前研究人员在文章中首次报道了免疫调节的铁死亡或会发生在肿瘤细胞内,而且还在癌症免疫疗法中扮演着关键角色。
这项最新研究中,研究人员发现,患者肿瘤样本中高水平的SLC13A3或与其对免疫疗法反应不良及患者较差的总体生存率有关,同时他们还在来自多个研究机构的多种类型癌症患者的肿瘤样本中进行了相关测试;随后他们在肿瘤中SLC13A3被敲除的小鼠模型中验证了这一发现,剔除SLC13A3就会导致肿瘤发生和进展减少,同时恢复SLC13A3的功能则会引起肿瘤进展,研究人员还注意到,相比表达SLC13A3的肿瘤细胞而言,肿瘤中SLC13A3被剔除的小鼠机体中的免疫细胞水平上升了。
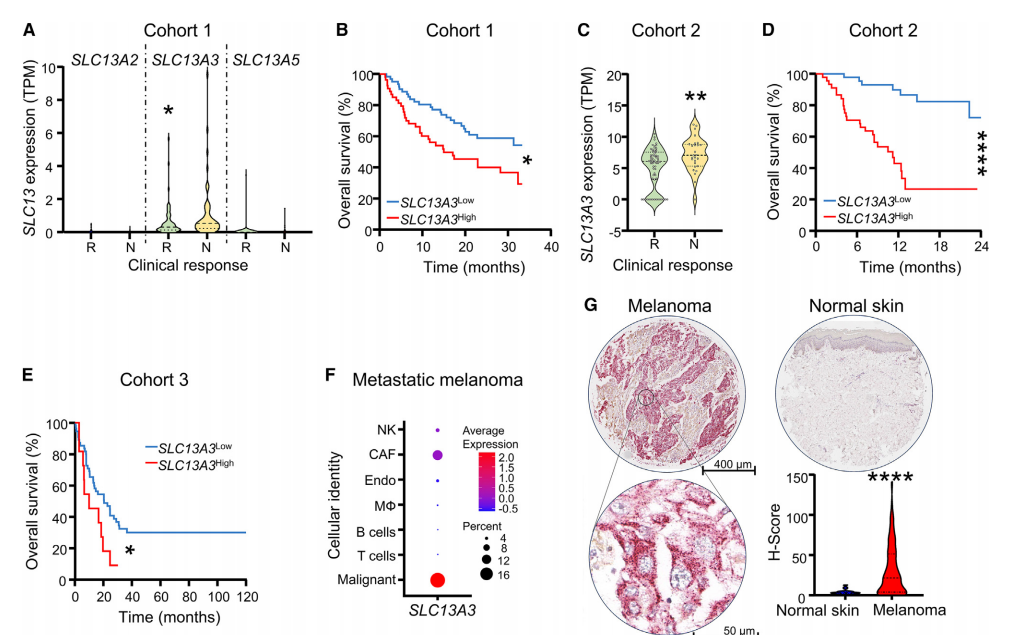
肿瘤中SLC13A3的表达与免疫检查点阻滞疗法的疗效及患者的生存相关
进一步研究后,研究人员发现了驱动这一现象的机制,即肿瘤细胞能利用SLC13A3来摄取一种称之为衣康酸的代谢产物,随后,衣康酸就能刺激铁死亡耐受机制并促使肿瘤细胞对铁死亡的细胞死亡形式耐受,从而对免疫疗法变得没有反应。衣康酸是由肿瘤微环境中的巨噬细胞所产生的,这就意味着,巨噬细胞和肿瘤细胞之间会通过SLC13A3来发生有害的串扰机制。
通过联合研究后,研究人员开发出了SLC13A3结构模型来筛选并识别除了潜在的抑制剂SLC13A3i,其能阻止肿瘤细胞摄取衣康酸并逆转对铁死亡的耐受,随后研究人员在小鼠机体中测试了这种抑制剂作为单一疗法或与免疫检查点抑制剂联合治疗时的疗效。SLC13A3抑制剂单独使用能逆转小鼠机体的铁死亡耐受并治疗癌症,而结合起来后,这两种抑制剂则能阻断肿瘤的进展并增强基于免疫的疗法在小鼠机体中的治疗疗效。
研究者Zou表示,我们的研究结果表明,SLC13A3在塑造肿瘤细胞的命运和基于免疫的癌症疗法的有效性方面发挥着重要作用,SLC13A3是一种开发临床适用的SLC13A3抑制剂的有希望的靶点,或有望促使基于免疫的疗法更有效地治疗更多癌症患者。
综上,本文研究中,研究人员识别出了肿瘤和肿瘤相关巨噬细胞之间通过SLC13A3-衣康酸-NRF2- SLC7A11轴所发生的相互作用,这或许能作为肿瘤微环境中此前未知的免疫铁死亡耐受机制,而且SLC13A3或许还能作为治疗SLC13A3+癌症的潜在免疫代谢靶点。(100yiyao.com)
参考文献:
Heng Lin,Kole Tison,Yuheng Du,et al. , Cancer Cell (2024). DOI:10.1016/j.ccell.2024.10.010.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载->
