Nature子刊:AI从头设计多肽,精准抑制细胞焦亡,开辟炎症疾病治疗新途径
时间:2025-09-18
来源:生物世界 2025-09-18 09:55
该研究利用人工智能(AI)从头生成了特异性阻断 GSDMD-NT 孔道的多肽——SK56,能够延缓细胞焦亡,减轻炎症反应,从而为不受控炎症引起或加重的人类疾病提供了新的治疗选择。gasdermin(GSDM)家族包括人类的 GSDMA 至 GSDME 等成员,它们通过在细胞膜上打孔,引发细胞焦亡(Pyroptosis)。在炎症性疾病中,GSDMD介导的细胞焦亡通过其N端片段(GSDMD-NT)在细胞膜上形成孔道,触发细胞裂解与细胞因子风暴,且可经细胞胞外囊泡传播至邻近细胞,加剧炎症扩散。
GSDMD-NT 孔道形成过程中的主要结构变化,使得难以获得稳定的 GSDMD-NT 孔道蛋白,从而阻碍了传统高通量筛选方法识别用于孔道阻断的先导分子,且其孔道直径达到了 21 纳米,这限制了小分子抑制剂的作用。此外,完全阻断GSDMD 会干扰其稳态功能,因此,开发可逆、封堵成熟孔道的配体,是当前的关键挑战。
2025 年 9 月 15 日,大坪医院与化学中毒全国重点实验室(现就职于中国科学院成都生物研究所)王淦研究员,昆明市延安医院云南省心重点实验室孟平副研究员和大坪医院创伤与化学中毒全国重点实验室曾灵研究员团队合作(孙剑会、杨俊为论文共同第一作者),在 Nature 子刊Nature Immunology上发表了题为:Delaying pyroptosis with an AI-screened gasdermin D pore blocker mitigates inflammatory response的研究论文。
该研究利用人工智能(AI)从头生成了特异性阻断GSDMD-NT 孔道的多肽 SK56,能够延缓细胞焦亡,减轻炎症反应,从而为不受控炎症引起或加重的人类疾病(例如脓毒症、慢性炎症和自身免疫性疾病)提供了新的治疗选择。

人工智能(AI)彻底改变了蛋白质设计领域,催生了诸如 RFDiffusion、MaSIF、RifDock 和 SCUBA 等众多方法,这些方法能够设计出高亲和力的结合蛋白。
在这项最新研究中,研究团队开发了基于 Transformer 的交互式界面原子生成式模型 TransForPep,进行虚拟多肽筛选,并进行优化和表征,从而从头生成了一种强效的 GSDMD-NT 孔道阻断剂 SK56。
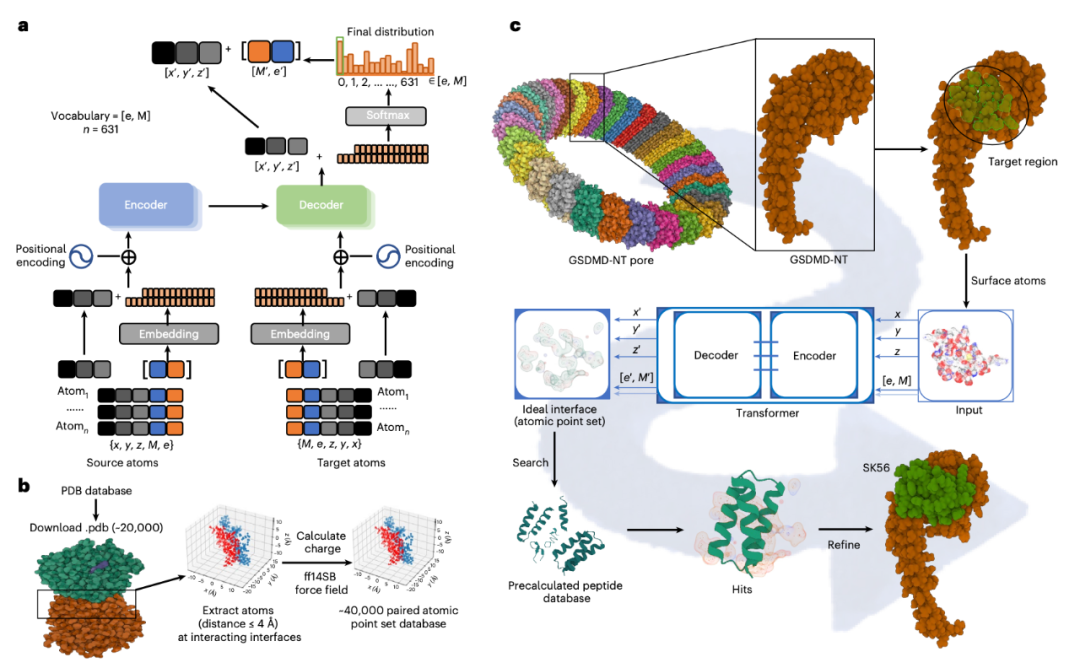
具体来说,SK56能够选择性靶向阻断GSDMD-NT 孔道,有效延缓细胞焦亡,并抑制巨噬细胞和人外周血白细胞诱导的细胞焦亡中的细胞因子释放。SK56 能防止脂多糖或盲肠结扎手术诱导的脓毒症小鼠的死亡。SK56 不影响白细胞介素-1 (IL-1 )或 GSDMD 的切割。相反,SK56 抑制焦亡巨噬细胞释放细胞因子,减轻由焦亡细胞膜孵育引发的原代小鼠树突状细胞的活化,并在类器官-巨噬细胞共培养模型中防止人肺泡类器官的因焦亡扩散引发的广泛细胞死亡。SK56 能阻断脂质双层纳米颗粒上的 GSDMD-NT 孔道,并进入焦亡巨噬细胞抑制线粒体损伤。SK56 为对抗多种炎症相关疾病提供了新的可能。
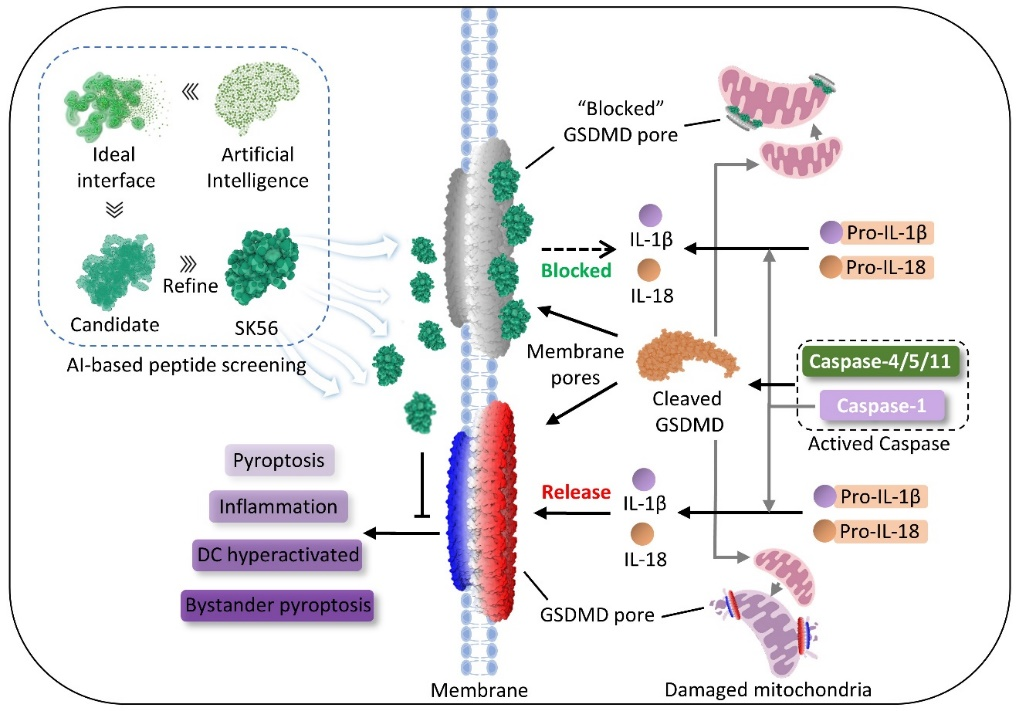
该研究展示了 AI 引导的多肽类设计在靶向 不可成药 生物结构中的潜力,为生物药物开发开辟了新途径。此外,该研究中筛选的多肽 SK56,可在焦亡反应开始后依然有效,这挑战了 焦亡一旦触发即不可逆 的传统认知。
这些研究结果可能为治疗由不受控炎症引起或加重的人类疾病提供了新的治疗选择,也让我们重新思考 人类或许能更聪明地 与炎症共处 ,而非 一味压制 。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载->
