Cell子刊:敲除这两个基因,提高CAR-T细胞治疗实体瘤的效果
时间:2025-08-22
来源:生物世界 2025-08-22 09:29
间皮素(MSLN)是实体瘤 CAR-T 细胞疗法的一个颇具吸引力的靶点,因为它在包括PDAC 在内的多种癌症中均过表达。此外,MSLN 水平升高与 PDAC 患者的不良预后相关,并且与肿瘤进展有关。晚期胰腺导管腺癌(PDAC)的患者中位生存期不足一年,这凸显了治疗方面迫切需要取得进展。
2025 年 8 月 19 日, 细胞疗法先驱Carl June教授团队等在 Cell 子刊Cell Reports Medicine上发表了题为:Clinical and molecular dissection of CAR T cell resistance in pancreatic cancer的研究论文。
该论文报告了一项 1 期临床试验,评估了抗 MSLN CAR-T 细胞疗法在晚期胰腺导管腺癌(PDAC)患者中的安全性和疗效。结果显示,该CAR-T 细胞疗法在患者中耐受性良好,但效果不佳。研究团队进一步在小鼠实验中生死,在这些 CAR-T 细胞中同时敲除ID3和SOX4可提高长期无复发生存率。

联合化疗是转移性胰腺导管腺癌(PDAC)的标准治疗方法,但总体疗效有限,PDAC 仍是致死率最高的之一。此外,尽管检查点阻断(ICB)疗法和 CAR-T 细胞疗法在其他多种癌症中取得了成功,但它们在 PDAC 中的疗效仍然有限。
间皮素(MSLN)是实体瘤 CAR-T 细胞疗法的一个颇具吸引力的靶点,因为它在包括PDAC 在内的多种癌症中均过表达。此外,MSLN 水平升高与 PDAC 患者的不良预后相关,并且与肿瘤进展有关。
该团队此前已开展了几项间皮素(MSLN)靶向的 CAR-T 细胞疗法的 1 期临床试验。首先,研究团队用经电导入了鼠源性抗人 MSLN ScFv SS-1 mRNA 的 T 淋巴细胞治疗了对化疗耐药的转移性 PDAC 患者。这使得 CAR 得到了短暂表达,并且在 5 名接受治疗的患者中有 2 名获得了病情稳定的最佳疗效。一项后续研究评估了基于 SS-1 的 CAR 在恶性、和胰腺导管腺癌患者中的稳定转导情况。尽管这种疗法能够耐受,但疗效有限,15 名患者中仅有 11 名病情稳定,其中包括 5 名 PDAC 患者中的 2 名。
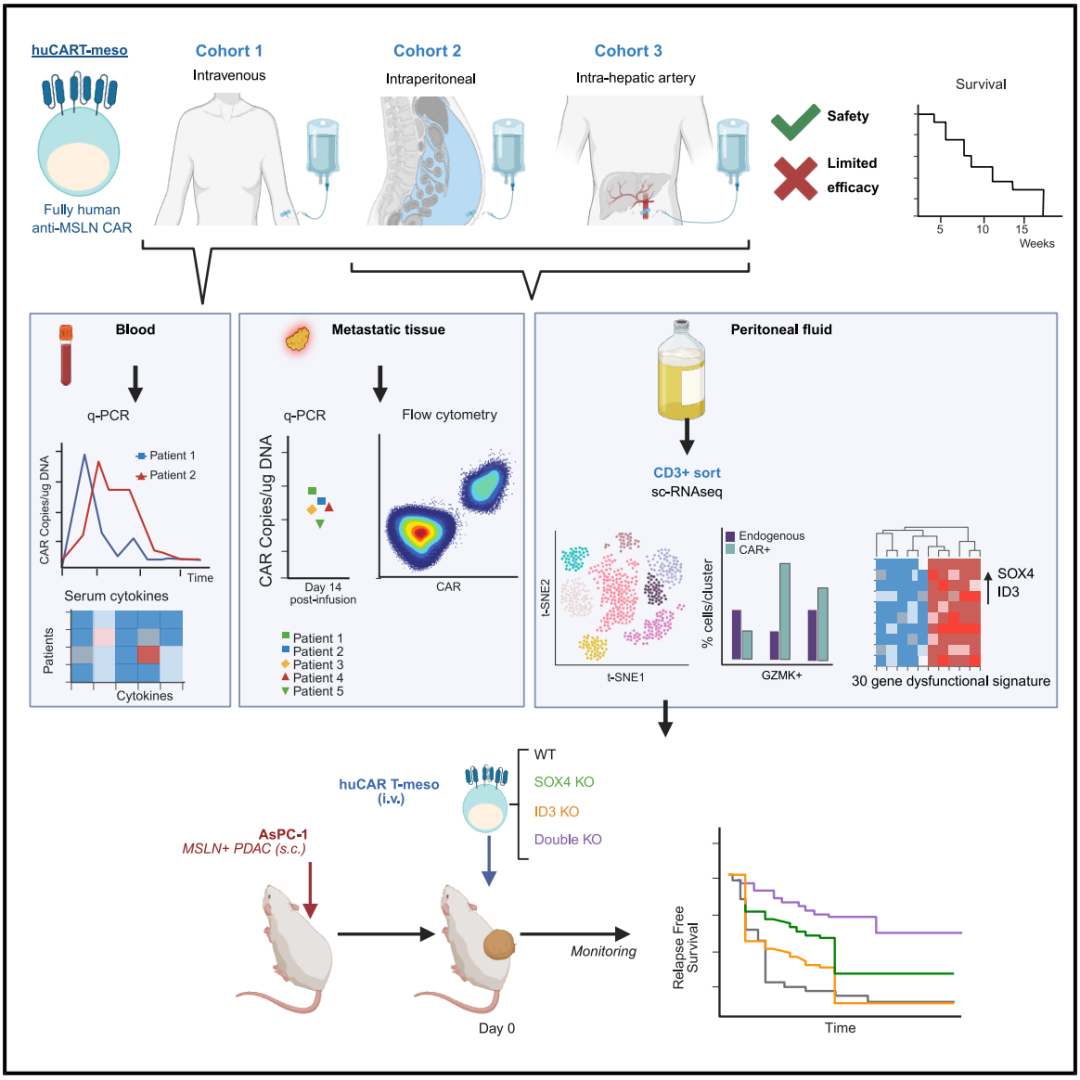
在该论文所述的 1 期临床试验中,研究团队评估了一种全人源抗 MSLN CAR 构建体(huCART-meso)在组织学确诊的转移性 PDAC 患者中的安全性和疗效。为了更好地理解治疗反应,研究团队报告了血液、腹水以及可评估转移灶的治疗前后配对活检的相关分析结果。研究团队还结合了体内小鼠模型和高通量基因组学实验,以深入了解 PDAC 患者对 CAR-T 细胞治疗产生耐药性的机制。
该1 期临床试验分三个组(每组 3 名患者),1 组通过输入 CAR-T 细胞,2 组通过腹腔输入 CAR-T 细胞,3 组通过肝动脉输入CAR-T 细胞。结果显示,CAR-T细胞耐受性良好,总体安全,未出现 3 级以上治疗相关不良事件。所有患者在转入长期随访前均已死亡。对于第 1 组,其中有 1 名患者在第 28 天时病情稳定,在第三个月时病情进展,所有3 名患者在转入临终关怀前退出了研究;在第 2 组和第 3 组中,所有 6 名患者在第 28 天时均出现病情进展,均在研究期间死亡,其中 5 名死于疾病进展,1 名死于急性肾损伤。患者的中位总生存期为 6.7 周,中位无进展生存期为 3.9 周。
单细胞基因组学方法揭示,输注后的 CAR-T 细胞表达耗竭标志物,包括先前已确定的转录因子ID3和SOX4,并且富含 GZMK+表型。在异种移植小鼠模型中,单独敲除 CAR-T 细胞的 ID3 或 SOX4 可增强疗效,但存在供体依赖性差异。单基因敲除细胞最终会失效,而 ID3 和 SOX4 双基因敲除的 CAR-T 细胞 则表现出更长的无复发生存期,这表明其具有持续的治疗效果,并为胰腺导管腺癌(PDAC)中设计更有效的 CAR-T 细胞提供了潜在途径。
该研究的核心发现:
抗 MSLN CAR - 细胞疗法在晚期胰腺导管腺癌患者中耐受性良好,但疗效有限;
转录组分析表明,输注道患者体内的的 CAR-T 细胞功能失调;
ID3 和 SOX4 双基因敲除的 CAR-T 细胞在体内诱导了长期无复发生存期。